Химические реакции играют важную роль во многих аспектах нашей жизни. Они происходят внутри нашего организма, в природных процессах, а также в промышленности. Скорость химической реакции является ключевым параметром, определяющим, насколько быстро реагенты превращаются в продукты. Концентрация реагентов является одним из факторов, влияющих на скорость реакции.
Концентрация представляет собой количество реагентов, содержащихся в единице объема или массы. Повышение концентрации реагентов обычно увеличивает скорость реакции. Это происходит потому, что с увеличением концентрации реагентов увеличивается вероятность их столкновений. Более высокая концентрация означает большее число реагентов в определенном объеме, что повышает вероятность столкновения молекул и, следовательно, увеличивает скорость химической реакции.
Для лучшего понимания роли концентрации в скорости химической реакции, рассмотрим примеры. Реакция между цинком и серной кислотой – классический пример, иллюстрирующий влияние концентрации реагентов на скорость реакции. При добавлении цинка к серной кислоте, начинается реакция, в результате которой выделяется водород. Если увеличить концентрацию цинка, то скорость реакции также возрастет. Это связано с тем, что большее количество цинка сталкивается с молекулами серной кислоты, что увеличивает число столкновений и, следовательно, скорость реакции.
Концентрация и скорость химической реакции
Концентрация одним из факторов, который оказывает влияние на скорость химической реакции. Концентрацию можно определить как количество вещества, содержащегося в единице объема.
При повышении концентрации реагентов происходит увеличение вероятности столкновений между частицами реагентов. Из-за увеличенной частоты столкновений возрастает вероятность эффективных столкновений, то есть таких столкновений, при которых происходит образование новых химических связей и образование продуктов реакции.
Пример 1: Рассмотрим реакцию между серной кислотой (H2SO4) и металлическим цинком (Zn). Если концентрация серной кислоты увеличивается, то скорость реакции также будет увеличиваться. Это происходит потому, что увеличенная концентрация серной кислоты приводит к увеличению количества доступных частиц, способных реагировать с цинком. В результате частота и скорость столкновений между реагентами увеличивается, что приводит к повышению скорости образования продуктов реакции.
Однако следует отметить, что при достижении определенного уровня концентрации, дальнейшее повышение концентрации может не привести к значительному увеличению скорости реакции. Это связано с тем, что на определенном этапе реагенты могут находиться в избытке, и большее количество реагентов не приведет к увеличению скорости образования продуктов реакции.
Другим важным аспектом влияния концентрации на скорость химической реакции является применение катализаторов. Катализаторы могут увеличить скорость реакции, не участвуя в реакционном уравнении. Они могут облегчить процесс столкновения реагентов и активировать определенные реакционные пути, ускоряя химическую реакцию. При использовании катализатора, концентрация самого катализатора также может оказывать влияние на скорость реакции.
Важно помнить, что изменение концентрации реагентов может привести к изменению не только скорости химической реакции, но и к изменению равновесия реакции. Поэтому при изучении влияния концентрации на реакцию следует учитывать и термодинамические аспекты процесса.
Влияние концентрации на скорость реакции
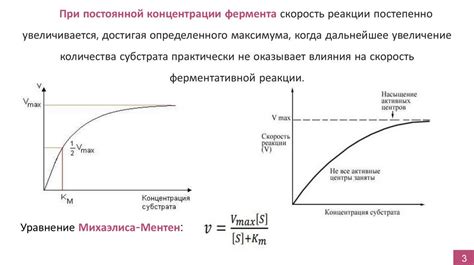
При увеличении концентрации реагентов количество сталкиваемых частиц увеличивается, что увеличивает вероятность их взаимодействия. Большее количество частиц создает больше возможностей для образования новых связей и образования продуктов реакции.
Если один из реагентов находится в избытке, то его концентрация не влияет на скорость реакции. Фактически, скорость реакции будет зависеть только от концентрации вещества, которое присутствует в недостаточных количествах.
Для некоторых реакций повышение концентрации может привести к возникновению побочных реакций или изменению пути реакции. Поэтому важно оптимально подобрать концентрацию реагентов, чтобы достичь желаемого результата в максимально короткий промежуток времени.
В дополнение к концентрации, на скорость реакции также влияют температура, давление, катализаторы и другие факторы. Чтобы полностью понять и оценить влияние концентрации на скорость реакции, необходимо провести серию экспериментов с разными значениями концентрации и анализировать их результаты.



